一种检测乙型流感病毒核酸的dna探针及其应用
技术领域
1.本发明涉及生物检测技术领域,具体是一种检测乙型流感病毒核酸的dna探针及其应用。
背景技术:
2.流感病毒属于正粘病毒科,是一种呼吸道病毒,通过气溶胶、飞沫传播,人群普遍易感,以发热、肌肉酸痛和鼻塞流涕等症状为主要临床表现。由于流感表现缺少特异性,难于与其他疾病区分,因此早期诊断乙型流感病毒对于开展病毒治疗及控制传染至关重要。
3.目前,临床诊断乙型流感病毒的金标准是逆转录聚合酶链式反应(rt-pcr)。然而,rt-pcr方法操作复杂、耗时、仪器设备要求高,同时对操作人员技术要求高,在偏远地区及小型医院难以开展现场即时检测(poct),因此有必要探索一种操作简便、快速同时兼具灵敏度和特异性的乙型流感病毒检测方法
技术实现要素:
4.本发明的目的在于提供一种检测乙型流感病毒核酸的dna探针及其应用,解决了上述技术问题,利用dna探针与目标rna混合催化发夹自组装反应结合免疫层析试纸条,在等温无酶扩增环境下即可快速、高灵敏度、高特异性地检测乙型流感病毒,实现乙型流感病毒现场即时检测。
5.本发明的目的可以通过以下技术方案实现:
6.一种检测乙型流感病毒核酸的dna探针,所述dna探针包括探针h1和探针h2,序列如下:
7.dna探针h1:
8.attggatgttactaccatgaggctccatttcactcgctcatggtagtaac
9.dna探针h2:
10.ccatgagcgagtgaaatggagcctcatggtagtaacgctccatttcactc
11.g
12.所述dna探针与目标rna混合进行催化发夹自组装反应。
13.进一步地,所述探针h1和探针h2均为发夹结构,探针h1的5’端由生物素修饰,探针h2的5’端由地高辛修饰。
14.进一步地,所述目标rna通过序列比对选择一段长度为21个碱基的保守序列。
15.进一步地,所述催化发夹自组装反应为dna探针与目标rna混合后目标rna触发反应形成h1/h2杂交双链。
16.检测乙型流感病毒核酸的dna探针的应用,所述dna探针应用于流感病毒核酸检测,具体包括以下步骤:
17.s1、根据目标rna设计dna探针
18.在ncbi流感数据库中下载乙型流感病毒序列,并通过mafft序列比对功能找到保
守序列,根据保守序列在nupack中设计发夹dna探针,发夹dna h1的5’端由生物素修饰,探针h2的5’端由地高辛修饰;
19.s2、dna探针与目标rna混合进行催化发夹自组装反应
20.取40-60μl探针h1、40-60μl探针h2、40-60μl目标rna混合,在25-40℃水浴锅中反应15-30min,反应产生h1/h2杂交双链;
21.s3、取70-80μl步骤s2中得到的反应液滴加于免疫层析试纸条,等待10-20min;
22.s4、将步骤s3中的免疫层析试纸条通过免疫层析定量分析仪检测荧光结果。
23.进一步地,所述步骤s2中探针h1和探针h2的浓度均为3nmol/l。
24.进一步地,所述免疫层析试纸条由样品垫、结合垫、硝酸纤维素膜和吸收垫构成。
25.进一步地,所述结合垫上包被有alexa fluor 647荧光素和链霉亲和素(sa)双标记的纳米微球,硝酸纤维素膜标有检测线和质控线;所述检测线处通过喷洒抗地高辛/地高辛单克隆抗体制备,质控线上涂抹生物素。
26.进一步地,所述dna探针与目标rna混合催化发夹自组装反应产物通过非还原性聚丙烯酰胺凝胶电泳和实时荧光监测验证。
27.进一步地,所述步骤s4通过检测单碱基突变rna和双碱基突变rna荧光值进行特异性分析;
28.单碱基突变rna序列:cucaugguaguuacauccaau
29.双碱基突变rna序列:cucgugguaguuacauccaau。
30.本发明的有益效果:
31.本发明利用dna探针与目标rna混合进行催化发夹自组装反应形成h1/h2杂交双链,联合免疫层析试纸条,通过非还原性聚丙烯酰胺凝胶电泳和实时荧光监测验证,可以在等温无酶环境下即可快速、高特异性、高灵敏度地检测乙型流感病毒核酸,实现乙型流感病毒现场即时检测,操作简单方便,检测成本低,降低医疗工作者检测难度。
附图说明
32.下面结合附图对本发明作进一步的说明。
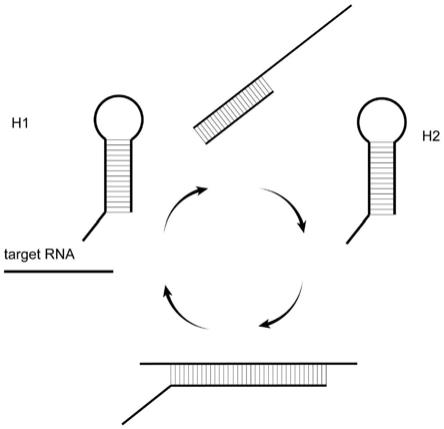
33.图1是本发明催化发夹自组装的反应原理示意图;
34.图2是本发明免疫层析试纸条检测地高辛和生物素双标记的h1/h2杂交双链原理示意图;
35.图3是催化发夹dna自组装用于检测乙型流感病毒的可行性分析结果示意图;
36.图4是本发明电泳验证催化发夹自组装检测乙型流感病毒可行性示意图
37.图5是本发明催化发夹dna自组装联合免疫层析试纸条检测系统的灵敏度分析结果示意图;
38.图6是本发明目标rna的浓度与荧光值成线性关系图;
39.图7是本发明催化发夹dna自组装联合免疫层析试纸条检测系统的特异性分析结果示意图。
具体实施方式
40.下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完
整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其它实施例,都属于本发明保护的范围。
41.一、检测探针冻干粉的制备
42.本发明目标rna通过mafft实现序列比对,筛选出乙型流感病毒基因中长度为21个碱基的保守序列为检测靶标,通过nupack软件设计dna探针,由其设计的探针分别为h1和h2,序列如下:
43.表1:乙型流感病毒目标rna及探针序列
[0044][0045]
探针h1和h2,分别用生物素(biotin)修饰h1的5’端,地高辛(digoxin)修饰h2的5’端,当目标rna存在时,由目标rna触发反应,依次打开发夹探针h1和探针h2,由于序列互补形成地高辛和生物素双标记的h1/h2杂交双链,如图1所示;
[0046]
将制备的探针溶解于tnak缓冲液(20
×
10-3
mol/ltris,ph 7.5;40
×
10-3
mol/l nacl;5
×
10-3
mol/lkcl),进行退火处理,将探针置于95℃水浴锅中,自然冷却至室温,使探针保持发夹结构,探针放置于-20℃备用。
[0047]
二、催化发夹dna自组装用于检测乙型流感病毒的可行性分析
[0048]
1、实时荧光定量pcr监测催化发夹自组装反应进程。
[0049]
探针h2标记荧光基团(fam)和淬灭基团(bhq1),由上海生工生物工程公司合成并纯化。取900nmol/l h1、900nmol/l h2、900nmol/l目标rna各10μl,设置反应温度为37℃,30秒一次循环,共80次循环,由cfx96real-time system检测。
[0050]
如图3所示,实时荧光定量曲线表明,不存在目标rna时,仅有与空白组接近的微弱荧光,当目标序列和探针同时存在时,探针h1和h2发夹依次被打开,最终形成大量h1/h2杂交双链,产生明显的荧光曲线。
[0051]
2、非变性聚丙烯酰胺凝胶电泳(native-page)验证催化发夹组装反应。
[0052]
配制12%的非变性聚丙烯酰胺凝胶,退火处理后的探针h1和h2及目标rna稀释至900nmol/l,取h1、h2、目标rna各10μl,混匀后在37℃水浴15分钟;
[0053]
加入4μl 6
×
上样缓冲液混合,取15μl混合液上样,在120v电压下电泳60分钟,电泳凝胶用eb染色10分钟,通过凝胶成像仪成像。电泳条带1-7分别:探针h1,探针h2,目标rna,探针h1+探针h2,探针h1+目标rna,探针h2+目标rna,探针h1+探针h2+目标rna。
[0054]
如图4所示,第4条泳道表明,在目标rna不存在时,所设计的两个探针h1和h2有微弱自发结合,第7条泳道表明,当加入h1、h2和目标rna即产生明亮的新条带,即h1/h2杂交双链。
[0055]
三、催化发夹dna自组装联合免疫层析试纸条检测系统的灵敏度分析
[0056]
目标rna用咽拭子病毒保存液稀释,浓度分别为1nmol/l、800pmol/l、600pmol/l、500pmol/l、400pmol/l、200pmol/l、100pmol/l、50pmol/l、10pmol/l、1pmol/l;
[0057]
取50μl不同浓度目标rna分别与50μl h1(3nmol/l)、50μl h2(3nmol/l)各50μl混匀,在25℃水浴锅中反应15分钟(探针h1和探针h2浓度最适比例为1:1,最适反应温度为25℃,已进行温度优化);
[0058]
取反应液75μl滴加至免疫层析试纸条,图2为免疫层析试纸条检测地高辛和生物素双标记的h1/h2杂交双链原理示意图,免疫层析试纸条由样品垫、结合垫、硝酸纤维素膜和吸收垫构成,结合垫上包被有alexafluor 647荧光素和链霉亲和素(sa)双标记的纳米微球,硝酸纤维素膜标有检测线(t线)和质控线(c线),检测线处通过喷洒抗地高辛/地高辛单克隆抗体制备,质控线上涂抹生物素,15分钟后在免疫荧光定量分析仪上读取检测线与质控线处荧光值。
[0059]
荧光结果如图5、图6所示,随着目标rna浓度降低,荧光值也随着降低,本研究最低可检测目标rna浓度为1pmol/l,目标rna的浓度与荧光值成线性关系,回归方程为y=11.64*x+1314,r2=0.9801。
[0060]
四、催化发夹dna自组装联合免疫层析试纸条检测系统的特异性分析
[0061]
根据目标rna设计了单碱基突变rna(sm)、双碱基突变rna(dm),序列如表2所示:
[0062]
表2:单碱基突变rna(sm)及双碱基突变rna(dm)序列
[0063]
namesequenceinformation(5
’‑3’
)smcucaugguaguuacauccaaudmcucgugguaguuacauccaau
[0064]
将两条序列分别用咽拭子病毒保存液稀释至3nmol/l,取50μl突变rna(3nmol/l)与50μl探针h1(3nmol/l)、50μl探针h2(3nmol/l)充分混匀,在37℃水浴锅中反应15分钟得到反应液;
[0065]
取反应液75μl滴加至免疫层析试纸条,15分钟后在免疫层析定量分析仪上读取检测线与质控线处荧光值。
[0066]
检测结果如图7所示,目标检测序列所测得荧光值与突变序列所测荧光值存在明显差异,结果表明该检测方法对于乙型流感病毒检测有较高的特异性。
[0067]
在本说明书的描述中,参考术语“一个实施例”、“示例”、“具体示例”等的描述意指结合该实施例或示例描述的具体特征、结构、材料或者特点包含于本发明的至少一个实施例或示例中。在本说明书中,对上述术语的示意性表述不一定指的是相同的实施例或示例。而且,描述的具体特征、结构、材料或者特点可以在任何的一个或多个实施例或示例中以合适的方式结合。
[0068]
以上显示和描述了本发明的基本原理、主要特征和本发明的优点。本行业的技术人员应该了解,本发明不受上述实施例的限制,上述实施例和说明书中描述的只是说明本发明的原理,在不脱离本发明精神和范围的前提下,本发明还会有各种变化和改进,这些变化和改进都落入要求保护的本发明范围内。
[0069]
[0070]
